سدیم کربنات (Sodium carbonate)
- توضیحات
- نظرات (0)
توضیحات
سدیم کربنات (Sodium carbonate)
ویژگیهای فیزیکی
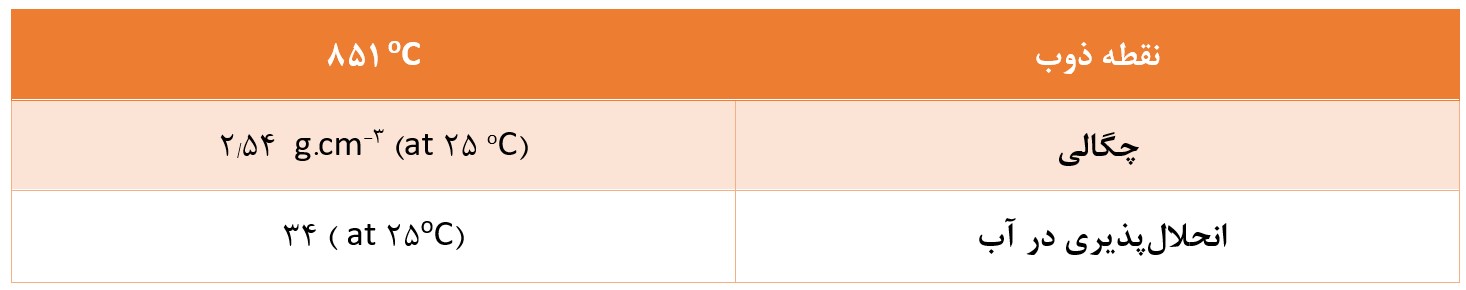
ویژگیهای کلی
توضیحات
سدیم کربنات یک ترکیب معدنی است. در شکلهای گوناگون ( آبدار و خشک) وجود دارد و در تمامی آنها سفیدرنگ، بی بو و محلول در آب است. و در آب خاصیت بازی (قلیایی) ضعیف ایجاد میکنند.
کاربردها
-به عنوان عامل پاککننده در پاککنندههای خانگی و برای مصرف عمومی مانند شستن لباس استفاده میشود. همچنین جز تشکیلدهنده صابونهای پودری است.
-برای از نرم کردن آب و از بین بردن موقت و یا دائمی آب استفاده میشود.
-در ساخت شیشه، صابون و کاغذ کاربرد دارد.
-در تولید ترکیبهای سدیم دار مانند بوراکس استفاده میشود.
-تولید شیشه
سدیم کربنات با اضافه شدن به سیلیکا نقش فلاکس ( اصطلاحی در علم مواد) را بازی میکند . با این کار نقطه ذوب آن را به یک مقدار قابل دسترسی تبدیل میکند.
ترکیب بدست آمده تا حدی در آب انحلالپذیر است. برای حل این مسئله به این مذاب، کلسیم کربنات اضافه میشود.
-نرمسازی آب
آب سخت ترکیبهای یونی کلسیم و منیزیم دارد. پ سدیم کربنات در آب محلول و کلسیم کربنات و منیزیم کربنات نامحلول هستند. با اضافه کردن آن به آب +Ca۲ و +Mg۲ حذف میشوند. این دو یون با یون کربنات ، ترکیبهای نامحلول در آب تشکیل میدهند و رسوب میکنند.
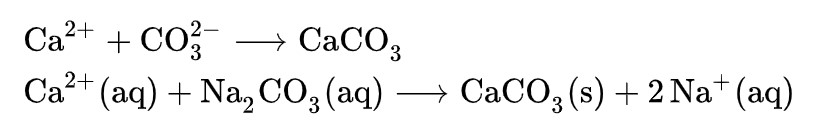
به این ترتیب آب نرم میشود.
-افزودنی در خوراکیها
سدیم کربنات نسبت به جوش شیرین برتر است. چرا که باز قویتری است. این روی گلوتن ( پروتئین موجود در برخی خوراکیها) تاثیر دارد و همچنین قهوهای شدن خمیر ورز داده شده را کاهش میدهد.
از سدیم کربنات در پودر شربت نیز استفاده میشود. حس خنکی و گازدار بودن آنها به علت واکنش گرمادهی است که بین سدیم کربنات و اسید ضعیف موجود در آنها رخ میدهد. چراکه این واکنش تولید کربن دی اکسید میکند.
همچنین در صنعت غذا به عنوان افزودنی به عنوان کنترلکننده اسیدیته، ضد کیک و پایدارکننده استفاده میشود.
-دیگر کاربردها
به علت خاصیت بازی در حوزههای گوناگون استفاده دارد. ارزانتر بودن آن نسبت به سدیم هیدروکسید باعث شده تا در فرایندهای شیمیایی بیشتر از آن استفاده شود.
به عنوان مثال، در تولید عاملهای تولید کننده فیلمهای عکاسی، نیاز به تنظیم pH است که از این ماده استفاده میشود.
همچنین در استخرها و آکواریومها برای تنظیم pH از آن استفاده میشود.
ماده اولیه برای تولید دیگر ترکیبها
سدیم بی کربنات یا به اصطلاح رایج جوش شیرین، یکی از اجزا موجود در کپسولهای اطفاء حریق است. این ماده معمولا از واکنش کربنات سدیم با کربن دی اکسید و آب تشکیل میشود. (معادله زیر)
Na۲CO۳ + CO۲ + H۲O → ۲NaHCO۳
در یک واکنش مشابه از این ماده برای سنتز سدیم بی سولفات نیز استفاده میشود. این ماده در جدا کردن لیگنین ( یک پلیمر طبیعی و بسیار پرمصرف) از سلولز کاربرد دارد.
Na۲CO۳ + SO۲ + H۲O → NaHCO۳ + NaHSO۳
-در صنعت پنبه نیز برای خنثیسازی سولفوریکاسید استفاده دارد.
–تهیه سدیم کربنات
روش رایج سنتز آن فرایند سولوی(Solvay) است.
واکنشهایی که در این فرایند انجام میشود به صورت زیر است
NaCl + NH۳ + CO۲ + H۲O → NaHCO۳ + NH۴Cl
۲NaHCO۳ → Na۲CO۳ + H۲O + CO۲
۲NH۴Cl + CaO → ۲NH۳ + CaCl۲ + H۲O
در واکنش سوم، در واقع آمونیاک مورد نیاز در واکنش شروع، بازتولید میشود.
تصویر زیر فرایند سالوی را نشان میدهد:
برای اطلاعات بیشتر در مورد این ماده اینجا کلیک کنید.
شما میتوانید برای تهیه انواع سدیم کربنات در وزنهای گوناگون با گروه شیمی تماس بگیرید.



















نقد و بررسیها
هنوز بررسیای ثبت نشده است.