سولفوریک اسید (Sulfuric Acid)
- توضیحات
- نظرات (0)
توضیحات
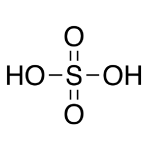
سولفوریک اسید (Sulfuric Acid)
ویژگیهای فیزیکی
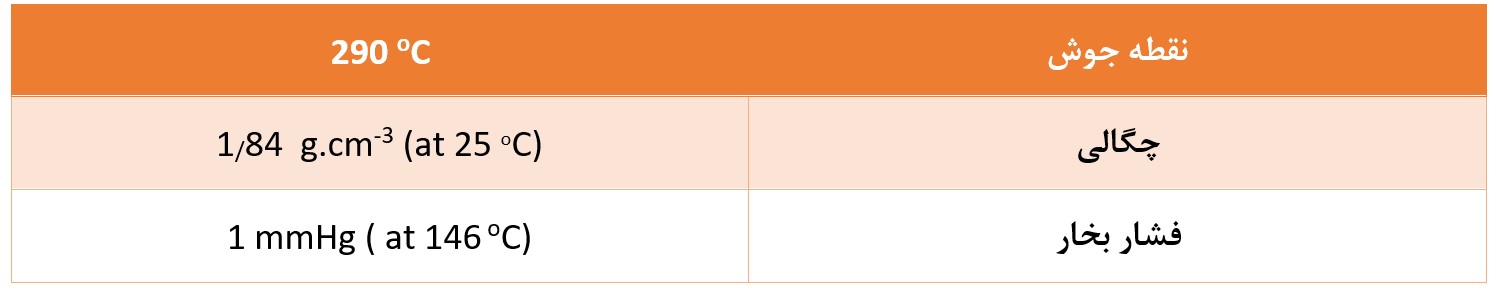
ویژگیهای کلی
مقدمه
سولفوریکاسید یک اسید معدنی است. مایعی بیرنگ، بی بو و امتزاجپذیر با آب است.
اسید سولفوریکاسید غلیظ یک خورنده بسیار قوی است. در حدی که فلزها، صخرهها و … را اکسید میکند.
واکنشپذیری بالایی با آب دارد و به همین دلیل برای اضافه کردن این دو، باید اسید را به آب اضافه کرد. در غیر این صورت گرمای زیادی آزاد میشود که میتواند محلول را تبخیر کند.
یک اسید بسیار مهم و کاربردی است. در حوزه تولید کود، تصفیه روغن، تصفیه آب و سنتز مواد شیمیایی کاربردهای فراوانی دارد.
در واکنشهای فراوانی نقش دارد که در ادامه به برخی از آنها اشاره میشود.
واکنش به عنوان اسید با بازها
در واکنش با بسیاری از بازها، تولید نمک سولفات میکند. به عنوان مثال از واکنش مس (II) اکسید با سولفوریکاسید، مس(II) سولفات تولید میشود.
CuO(s) + H۲SO۴(aq) → CuSO۴(aq) + H۲O(l)
به همین ترتیب در واکنش با سدیم استات، سدیم بی سولفات و در واکنش با پتاسیم نیترات، نیتریک اسید تولید میشود.
-در کنار نیتریک اسید در واکنشهای جانشینی هستهدوستی در ترکیبهای آروماتیک ایفای نقش میکند.
واکنش با فلزها
واکنش آن با فلزها از نوع جانشینی یگانه است و نمک مربوط و گاز هیدروژن تولید میکند (واکنش زیر)
Fe + H۲SO۴ → H۲ + FeSO۴
اکسنده
از سولفوریکاسید غلیظ به عنوان اکسیدکننده استفاده میشود. (واکنش زیر)
C + 2 H۲SO۴ → CO۲ + ۲ SO۲ + ۲ H۲O
سدیم بی سولفات از واکنش این اسید با سدیم کلرید سنتز میشود.
S + 2 H۲SO۴ → ۳ SO۲ + ۲ H۲O
جانشینی الکتروندوستی
در واکنش با بنزن، سولفونیک اسیدهای مربوط را میتواند تولید کند
آبگیری
یکی از کاربردهای مهم آن، خروج آب یا دی هیدراته کردن است. ویدیو زیر واکنش سولفوریکاسید با ساکاروز را نشان میدهد.
معادله واکنش آن به صورت زیر است:
C۱۲H۲۲O۱۱ + ۲۴H۲SO۴ → ۲۴SO۲ + ۱۲CO۲ + ۳۵H۲O
همچنین این اسید، در بسیاری از واکنشها در نقش کاتالیزگر واکنش را پیش میبرد. به عنوان مثال واکنش حذف E1 ، E2 ، آب دار شدن آلکنها و …
برای اطلاعات بیشتر در مورد این ماده اینجا کلیک کنید.
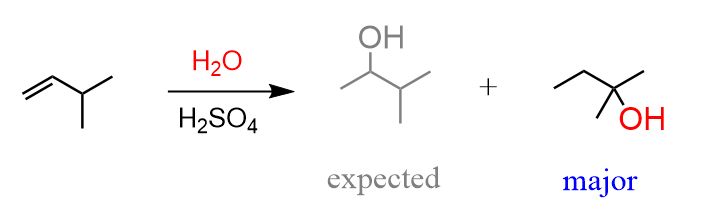
آبدار شدن آلکنها
حذف E1
حذف E2
برای اطلاعات بیشتر در مورد این ماده اینجا کلیک کنید.
شما میتوانید برای تهیه سولفوریک اسید در حجمهای گوناگون با گروه شیمی تماس بگیرید.
















نقد و بررسیها
هنوز بررسیای ثبت نشده است.